メッシュトラブル
腹圧性尿失禁(SUI)は、咳やくしゃみなどの動作によって引き起こされる尿漏れであり、18歳以上の女性の約3人に1人が影響を受け、生活の質(QOL)に大きな影響を与えます。最初の外科的治療法として、中部尿道スリング(MUS)の挿入が行われます。MUSには、無張力膣テープ(TVT)、経閉鎖孔テープ(TOT)、および中部尿道組織固定システム(TFS)の3種類があります。別の治療法としては、筋膜スリング手術があり、筋膜がメッシュの代わりに挿入されます。MUSは高い患者満足度が報告されていますが、5年間で2.7〜9.8%の合併症率があります。合併症の治療にはMUSの除去(実施率:約3%)および再挿入手術(実施率:2.7〜7.8%)が含まれますが、合併症率に比べてMUS除去を受ける人の割合は少ないです。合併症の中で、メッシュに関連する痛みはその後のQOLに大きな影響を与える可能性があり、MUS除去の1〜17%を占めます。MUS関連の訴訟の主な理由は、経膣メッシュ挿入後の痛みです。
メッシュ除去の主な適応症は、痛み、尿道閉塞、膣上皮侵食、および性交痛です。しかし、MUS手術後の痛みは、保守的な治療では管理が難しい場合が多く、侵食や露出などの明確な原因を除いては保守的な治療が成功することはほとんどありません。保守的な治療には、骨盤底筋運動、経口抗炎症鎮痛薬、および鎮痛薬および麻酔薬による局所麻酔が含まれます。その後、保守的な治療が失敗した場合、MUS除去が一定の成功を期待されますが、メッシュ除去に関する研究はほとんどありません。既存の研究では、メッシュ除去が過小評価されていることが示唆されています。これは主に、一部の医師または患者がメッシュ除去がSUIの再発や他の副作用を引き起こすと信じているためかもしれません。メッシュの問題は広範であり、米国食品医薬品局(FDA)は2011年に警告を発しました。
我々は、安全で効果的なサポート方法がメッシュ除去後のオプションとして存在すれば、メッシュの問題を抱える女性にメッシュ除去を積極的に推奨できると仮定しました。我々の選択肢には、非アブレーティブのエルビウム・イットリウム・アルミニウム・ガーネット(Er)SMOOTH®レーザーが含まれ、膣(膣エルビウムレーザー(VEL))および尿道(尿道エルビウムレーザー(UEL))に特化したレーザーが付属しています。以前の報告では、VELとUELの組み合わせが重度のSUIを改善することが示されています。VEL自体は非常に安全で、副作用はほとんど観察されていません。重度のSUIの症例では、VELとUELの組み合わせ治療が行われ、MRIでの変化と尿道周囲の均一化が確認されました。VELおよびUELの効果は、2940 nmのSMOOTH Erレーザーを使用し、高い水親和性を持つものです。VELおよびUELは、約400〜500 µmの深さに熱浸透を提供する一連の非アブレーティブマイクロパルスを使用し、組織再生、コラーゲン形成、および血管発達を刺激します。このプロセスは表面損傷を伴わず、粘膜内で最大2 mmの深さまで影響を与えることが観察されています。
尿道メッシュ
48歳の女性(1回の妊娠・1回の出産)で、BMIは22.5 kg/m²でした。SUIのためにTOT MUSを受けた2年後に治療されました。TOTは中部尿道から左右の閉鎖孔スペースに挿入されました。
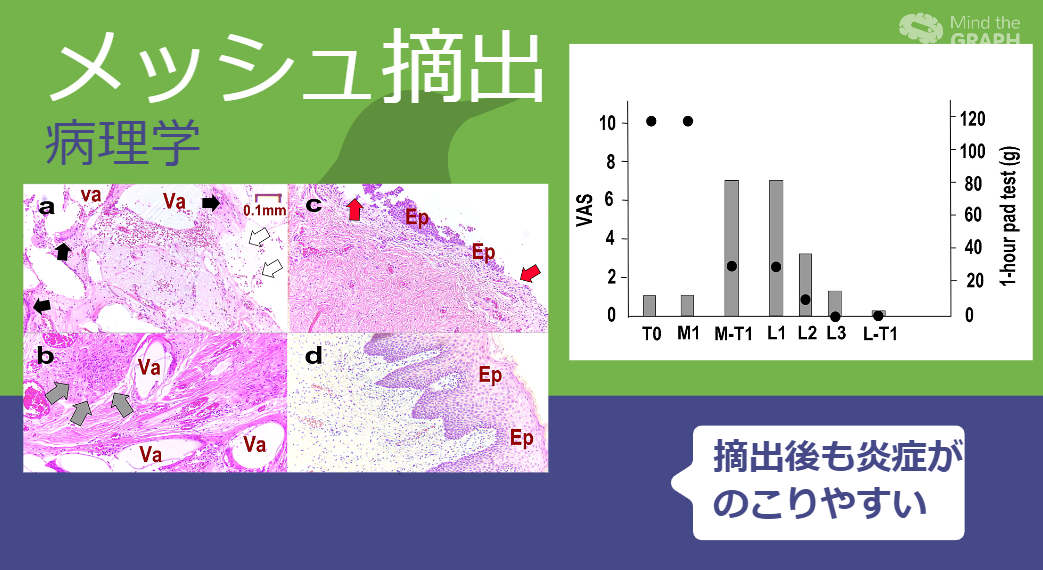
最初の受診時(T0)には、痛みは視覚的アナログスケール(VAS)で評価され、0から10の範囲で測定されました。VASの10は最も痛く、0は痛みがないことを意味します。T0時点で、中部尿道のメッシュに沿っておよび尿道の左右の膣壁に圧痛があり、VASスコアは10点でした。患者の日記には「ナイフが刺さっているような感覚」と繰り返し書かれていました。1時間のパッドテストでは、10gの漏れがありました。国際尿失禁質問票ショートフォーム(ICIQ-SF)スコアは7点でした。患者は右乳がんの腫瘍切除術を受けており、化学療法は受けておらず、女性ホルモン補充療法は禁止されていました。
本症例シリーズでは、すべての症例が同じ治療プロトコルに従いました。MUS除去およびレーザー療法の主な評価項目は痛みの緩和であり、副次的評価項目はSUIの治療でした。MUSの除去(M1)は2017年から2018年にかけて行われました。患者は最後のMUS除去手術(M-T1)から1年後に評価されました。再発したSUI患者には、骨盤底筋運動(骨盤底筋トレーニング(PFMT))と局所エストロゲン療法(LET)が6か月間処方されました。ただし、症例1のように禁忌のある患者にはLETを推奨しませんでした。持続的なSUIを経験している患者は、研究に参加し、VEL+UEL治療を受けました。VEL+UEL治療は、1か月間隔で3回のセッション(L1、L2、L3)で構成されていました。L3の1年後に痛みとSUIが再評価されました(L-T1)。MUS除去はすべての患者に対して同様の手順で行われましたが、各症例に応じてカスタマイズされました。VEL+UEL治療はすべての患者に対して症例1と同じプロトコルで実施されました。
MUS除去およびVEL+UEL治療には、治療開始前にすべての患者からインフォームドコンセントを取得し、手書きの署名を確保しました。
M1に最も影響を与えたパラメータは痛みの場所でした。これらの選択は外科医の裁量に委ねられました。痛みの場所に加えて、メッシュと尿道の解剖学的関係も考慮されました。
M1手順の例を示しています。麻酔前に痛みのある領域を確認しました。図1aでは、痛みが局所化しており、その領域の膣壁が硬くなっていることが観察されました(白い矢印)。その後、腰部麻酔が行われました。図1bでは、介入前に、病理組織診断のために上皮からメッシュまでのサンプルが切除されました。膣壁の痛みのある部分に沿って切開が行われ、メッシュが露出されました(灰色の矢印)。これらの手順は、周囲の組織に最小限の損傷を与えるように行われました。除去後、膣壁が閉じられました。図1cは症例1のMUS標本を示しています。
VEL+UEL治療では、最初にVELが行われ、直後にUELが続きました。VELのために、膣、陰唇、および尿道がヨウ素で消毒されました。8%キシロカインスプレー(サンドズKK、東京、日本)が麻酔のために15分間適用されました。レーザー照射はRenovalase(SP Dynamis Fotona d.o.o、リュブリャナ、スロベニア、図2a)で行われ、最初にVEL、次にUELが続きました。準備されたデバイスには、PS03、R11、およびR09-2 Guレーザープローブ用の特別なガラス膣鏡が含まれており、手持ち器具(PS03、R11、およびR09-2 Gu用の図2b)が含まれていました。各手持ち器具はSP Dynamisレーザーに接続されました。VELステップでは、ガラスのスペキュラムが膣に挿入され(図2c)、PS03レーザープローブで前膣壁が7 mmのスポットサイズ、6 J/cm²のパルスフルエンス、および2.0 Hzの周波数でスキャンされました(図2d)。この手順は5 mmごとに繰り返されました。次に、R11レーザープローブが使用され、360度の膣管全体に5 mm間隔でレーザー治療が適用されました。この治療はスポットサイズ7 mm、パルスフルエンス3.00 J/cm²、周波数2.0 Hzで行われました(図2e)。この手順は2回繰り返されました。UELには、R09-2 Guレーザープローブがカテーテル経由で使用され、膀胱から残尿を排出した後に行われました。レーザー治療の設定は、R09-2 Gu、SMOOTH、1.4 Hz、1.5 J/cm²、および2.5 mm間隔で尿道口から近位端まで4スタック行われました(図2f)。この治療は4回繰り返されました。VEL+UELの全プロセスは約30分で完了しました。VEL+UEL治療は1か月間隔で3回行われ(L1、L2、L3)、L3の1年後に痛みとSUIが再評価されました(L-T1)。
MUS除去のために、前膣壁に縦切開を行い、メッシュとアンカーを完全に除去しました(M1)。患者は最後のMUS除去手術(M-T1)から1年後に評価されました。
病理学を示しています。図4a、bはM1時点の病理組織を示しています。人工メッシュが存在した部分には多数の空胞が観察され、その周囲には多核巨大細胞が見られました(黒い矢印)。上皮は剥離しています(白い矢印)。図4cでは、空胞は消失しましたが、部分的な粘膜欠損が見られ(赤い矢印)、上皮の再生が不十分です。図4dでは、正常な粘膜が増殖しており、多核巨大細胞および空胞は観察されません。




